در دسامبر سال 2019، شیوع گسترده بیماری ویروس کرونا ویروس (COVID–19) در ووهان چین رخ داد و به سرعت در سایر کشورها گسترش یافت. این کلاس جدید از ویروس کرونا، معروف به سندرم حاد تنفسی حاد کرونا ویروس (SARS-CoV-2)، میتواند باعث عفونت های حاد تنفسی شده و به راحتی از انسانی به انسان دیگر منتقل شود. بنابراین، برای تشخیص موارد مثبت، به یک آزمایش سرولوژی ساده و سریع نیاز است.
میزان بالای انتقال COVID-19 مردم را وادار کرده است تا زمانی که امکان جلوگیری از شیوع بیشتر بیماری وجود ندارد، در خانه بمانند. به دلیل تعداد زیاد موارد بدون علامت و از آنجا که مطالعات اپیدمیولوژیک زیادی در این مورد صورت نگرفته است؛ بررسی میزان عفونت و کنترل موثر همه گیری مورد نیاز است.
در این شرایط، تشخیص سریع و درست این بیماری برای جلوگیری از همه گیری و نجات جان افراد از اهمیت بالایی برخوردار است. بر این اساس، آزمایش های مختلف تشخیصی مبتنی بر روش های تشخیص مولکولی و سرولوژیکی ایجاد شده است که برخی از تست ها و کیت های تشخیصی در بازار ارائه می شود. در میان آنها، روش های تشخیص به طور گسترده ای مورد استفاده قرار میگیرند که آزمایش ترجیحی برای تشخیص SARS-CoV-2 میباشد.
با وجود نتایج مناسب تشخیص COVID-19 توسط روش RT-PCR ، این آزمون وقت گیر، پرهزینه و به نیروهای آموزش دیده و تجهیزات اختصاصی نیاز دارد. در حقیقت، موارد بسیاری وجود دارد که دارای علایم بالینی بیماری هستند یا نتایج توموگرافی قفسه سینه (CT) خاصی دارند اما با این روش تشخیص داده نمی شوند.
این به دلیل غلظت ویروسی متغیر، انواع مختلف نمونه، روش های مختلف نمونه برداری، زمان مختلف نمونه برداری (در مراحل اولیه یا اواخر عفونت)، حفاظت و حمل و نقل نمونه ها، اهداف مختلف ژنی و غیره است.
آزمایشات سرولوژی که افزایش قابل توجه در آنتی بادی های IgG و IgM اختصاصی را در سرم بیماران اندازه گیری میکنند، آزمایش های مکمل خوبی برای آزمایش RT-PCR برای تشخیص بیماران COVID-19 هستند و در ارزیابی وضعیت ایمنی افراد بسیار ارزشمند هستند.
علاوه بر این، با استفاده از داده های سرولوژیکی می توان اطلاعات مهم اپیدمیولوژیک را جمع آوری کرد و وضعیت بیماری را با اطمینان بیشتری پیگیری نمود. در واقع، یافتن آنتی بادی های خاص علیه ویروس نقش مهمی در واکسن و فرآیند های تولید دارو دارد. بعلاوه، این آزمایشات سریع، اقتصادی و آسان انجام می شوند و همچنین نیازی به کارکنان آموزش دیده یا تجهیزات ویژه ندارند.
آنتیبادی IgM بین 7-10 روز پس از شروع علائم بیماری بروز میکند و معمولاً پس از 20 روز کاهش می یابد، تا زمانی که از بین برود. آنتیبادی IgG از روز 14 تا 20 پس از شروع علائم بیماری مثبت می شود و معمولاً برای مدت طولانی حفظ می شود.
بنابراین این روش تشخیصی برای ارزیابی پروسه درمان و همچنین واکسیناسیون و ایمنی پس از آن مفید باشد. بر این اساس، وجود IgM در سرم بیمار به معنای عفونت جدید یا مرحله اول عفونت است. اگر هر دو آنتی بادی IgM و IgG مثبت باشند ، بیمار در مرحله دوم عفونت است. اگر فقط IgG مثبت باشد، بیمار در آخرین مرحله بیماری است یا این بدان معناست که فرد برای مدتی در گذشته نزدیک بیمار بوده است. با این حال، لازم به ذکر است که از آنجا که افزایش آنتی بادی های ضد ویروسی حدود 7 روز پس از عفونت رخ می دهد، آزمایشات سرولوژیک آزمایش مناسبی برای تشخیص به موقع ویروس نیست در حالی که برای پیشگیری و مدیریت بیشتر بیماری بسیار مفید می باشد. نمودار افزایش و کاهش ایمنوگلوبولین ها از ابتدای عفونت در شکل 1 آمده است.
کیت تشخیص سریع آنتی بادی IgM و IgG کرونا ویروس جدید (COVID–19) شرکت آروین زیست سلامت برای تشخیص کیفی و تمایز آنتی بادی های IgM و IgG در سرم، پلاسما (EDTA، سیترات) یا خون کامل به کار میرود.
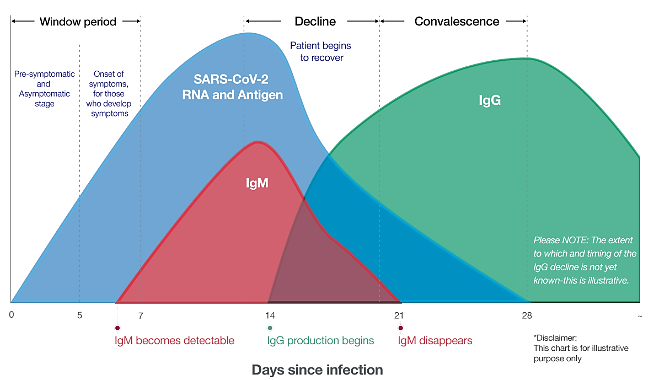
شکل شماره 1: نمودار افزایش و کاهش ایمنوگلوبولین ها از ابتدای عفونت
. Boes, Marianne. 2000. ‘Role of natural and immune IgM antibodies in immune responses’, Molecular immunology, 37: 1141-49.
2. Broughton, James P, Xianding Deng, Guixia Yu, Clare L Fasching, Venice Servellita, Jasmeet Singh, Xin Miao, Jessica A Streithorst, Andrea Granados, and Alicia Sotomayor-Gonzalez. 2020. ‘CRISPR–Cas12-based detection of SARS-CoV-2’, Nature Biotechnology: 1-5.
3. Chan, Jasper Fuk-Woo, Cyril Chik-Yan Yip, Kelvin Kai-Wang To, Tommy Hing-Cheung Tang, Sally Cheuk-Ying Wong, Kit-Hang Leung, Agnes Yim-Fong Fung, Anthony Chin-Ki Ng, Zijiao Zou, and Hoi-Wah Tsoi. 2020. ‘Improved molecular diagnosis of COVID-19 by the novel, highly sensitive and specific COVID-19-RdRp/Hel real-time reverse transcription-PCR assay validated in vitro and with clinical specimens’, Journal of clinical microbiology, 58.
4. Fang, Yicheng, Huangqi Zhang, Jicheng Xie, Minjie Lin, Lingjun Ying, Peipei Pang, and Wenbin Ji. 2020. ‘Sensitivity of chest CT for COVID-19: comparison to RT-PCR’, Radiology: 200432.

